Un poco de información previa
¿Qué son ácidos y bases ?
Los ácidos y bases son dos tipos de sustancias que de una manera sencilla se pueden caracterizar por las propiedades que manifiestan.
Los ácidos :
- tienen un sabor ácido
- dan un color característico a los indicadores (ver más abajo)
- reaccionan con los metales liberando hidrógeno
- reaccionan con las bases en proceso denominado neutralización en el que ambos pierden sus características.
Las bases :
- tienen un sabor amargo
- dan un color característico a los indicadores (distinto al de los ácidos)
- tienen un tacto jabonoso.
En la tabla que sigue aparecen algunos ácidos y bases corrientes :
| ácido o base | donde se encuentra |
| ácido acético | vinagre |
| ácido acetil salicílico | aspirina |
| ácido ascórbico | vitamina C |
| ácido cítrico | zumo de cítricos |
| ácido clorhídrico | sal fumante para limpieza, jugos gástricos |
| ácido sulfúrico | baterías de coches |
| amoníaco (base) | limpiadores caseros |
| hidróxido de magnesio (base) | leche de magnesia (laxante y antiácido) |
NOTA DE SEGURIDAD
NO se debe probar ningún ácido o base a menos que se tenga la absoluta certeza de que es inocuo. Algunos ácidos pueden producir quemaduras muy graves.
Es peligroso incluso comprobar el tacto jabonoso de algunas bases. Pueden producir quemaduras.
¿Qué es el pH ?
Los químicos usan el pH para indicar de forma precisa la acidez o basicidad de una sustancia. Normalmente oscila entre los valores de 0 (más ácido) y 14 (más básico). En la tabla siguiente aparece el valor del pH para algunas sustancias comunes.
| sustancia | pH | sustancia | pH |
| jugos gástricos | 2,0 | amoníaco casero | 11,5 |
| limones | 2,3 | leche de magnesia | 10,5 |
| vinagre | 2,9 | pasta de dientes | 9,9 |
| refrescos | 3,0 | disolución saturada de bicarbonato sódico |
8,4 |
| vino | 3,5 | agua de mar | 8,0 |
| naranjas | 3,5 | huevos frescos | 7,8 |
| tomates | 4,2 | sangre humana | 7,4 |
| lluvia ácida | 5,6 | saliva (al comer) | 7,2 |
| orina humana | 6,0 | agua pura | 7,0 |
| leche de vaca | 6,4 | saliva (reposo) | 6,6 |
¿Qué es un indicador ?
Los indicadores son colorantes orgánicos, que cambian de color según estén en presencia de una sustancia ácida, o básica.
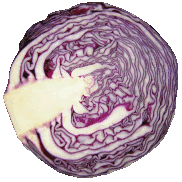
Fabricación casera de un indicador
Las lombardas, parecidas a repollos y de color violeta, contienen en sus hojas un indicador que pertenece a un tipo de sustancias orgánicas denominadas antocianinas.
Para extraerlo :
- Corta unas hojas de lombarda (cuanto más oscuras mejor)
- Cuécelas en un recipiente con un poco de agua durante al menos 10 minutos
- Retira el recipiente del fuego y dejarlo enfriar
- Filtra el líquido (Se puede hacer con un trozo de tela vieja)
- Ya tienes el indicador (El líquido filtrado)
Las características del indicador obtenido son :
| color que adquiere | medio en el que está |
| rosa o rojo | ácido |
| azul oscuro | neutro |
| verde | básico |
NOTA DE SEGURIDAD
El amoníaco es muy irritante. Debe Identifica adecuadamente el recipiente que lo contiene. NO debe probarse y NO debe dejarse en un sitio donde alguien pudiera probarlo por error.
Test de respiración (para gastar una broma)
Dale a alguien un vaso que contiene un poco de agua con extracto de lombarda y unas gotas de amoniaco casero y pídele que sople a través de una pajita de refresco. Puedes presentarlo como un test de alcohol, mal aliento, etc. La disolución pasará de color verde esmeralda a azul oscuro. Si ahora le añades vinagre, la disolución adquirirá un color rojo.
Al soplar expulsamos dióxido de carbono (CO2) que en contacto con el agua forma ácido carbónico (H2CO3). Este ácido formado, neutraliza el amoníaco que contiene la disolución. Al añadir vinagre la solución adquiere un pH ácido.
Cómo generar lluvia ácida
Impregna una tira de papel de cocina en una disolución del extracto de lombarda. Acerca una cerilla inmediatamente después de encenderla. Se observa que aparece un punto rojo (ácido) en la tira de papel.
¿A qué se debe ? ¿Puede ser debido al dióxido de carbono (CO2) generado en la combustión? No, la disolución formada (ácido carbónico) no es suficientemente ácida como para producir el color rojo. (Se puede comprobar repitiendo el
experimento pero dejando arder la cerilla un poco antes de acercarla al papel). La causa de la aparición del color rojo está en el dióxido de azufre (SO2) que se forma cuando la cerilla se inflama.
Esto se debe a la presencia de azufre (S) añadido, entre otros productos, a la cabeza de la cerilla, para favorecer la ignición.
El dióxido de azufre en contacto con el agua presente en la tira de papel forma ácido sulfuroso (H2SO3) que es más ácido que el ácido carbónico.
En la combustión de algunos derivados del petróleo se produce dióxido de azufre que pasa a la atmósfera. Al llover y entrar en contacto con el agua, se forma el ácido sulfuroso , uno de los responsables de la lluvia ácida.
Más información en SNYDER, C.H., 1995.The Extraordinary Chemistry of Ordinary Things. (John Wiley: New York)
La imagen de la lombarda esta modificada de una original de Rick Heath. Licencia Creative Commons Attribution 2.0 Generic license
